В апреле 2014 года Всемирная организация здравоохранения опубликовала доклад, в котором ее эксперты предупредили о грозящей человечеству опасности: отсутствие действенных антибиотиков сделает весьма сложными, либо вообще невозможными многие стандартные медицинские вмешательства, такие как хирургические операции, химиотерапия, трансплантация органов и даже лечение мелких травм и ожогов.
Что привело к такому положению дел? Прежде всего, чрезмерное использование антибиотиков, способствовавшее развитию штаммов микроорганизмов, обладающих резистентностью к этим препаратам, иными словами, супербагов. (Подробно о них читайте в нашей статье «Нас могут убить супербаги»).
Ученые-медики постоянно ведут исследования в этой актуальной области, и сегодня мы расскажем о некоторых из их последних изысканий. У нас есть одна плохая и три хороших новости на эту тему, причем две из них – весьма экзотические.
Но начнем с плохой.
Не только антибиотики способствуют росту резистентности
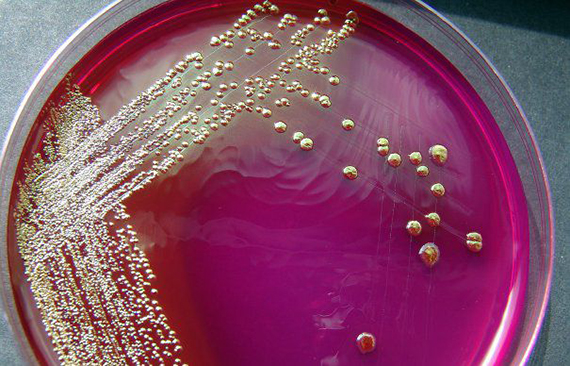
В марте 2018 года была опубликована работа группы немецких ученых, проведенная на базе Европейской лаборатории молекулярной биологии (EMBL). В своем исследовании они установили, что на бактерии влияют не только антибиотики, но и множество других медикаментов: антивирусные, антипсихотики, ингибиторы протонной помпы, химиотерапевтические средства и препараты, понижающие давление.
Прежде всего, ученые обнаружили, что эти лекарства влияют на состав кишечной микрофлоры организма, нарушая ее баланс. Но самой удивительной находкой оказалось то, что одни и те же бактерии обладали высокой устойчивостью как к антибиотикам, так и к тем лекарствам, которые должны были влиять на клетки организма человека.
Исследователи провели эксперимент со штаммом эшерихии коли (E coli), несущей ген резистентности к антибиотикам tolC. Этот ген продуцирует белок, который выталкивает антибиотики и другие химические агенты из бактериальной клетки. Бактерии E coli с повышенной экспрессией гена (то есть, производящие избыточное количество такого белка) продемонстрировали резистентность как к антибиотикам, так и к шести другим препаратам, в то время как E coli без этого гена оказались чувствительными к обеим группам.
В процессе эксперимента выяснилось, что и другие гены, ранее ассоциированные с антибиотикорезистентностью, также играли определенную роль в устойчивости к лекарствам другого назначения.
Полученные данные вызывают беспокойство у авторов работы. Весьма вероятно, что человек, принимающий препарат для понижения кислотности желудка либо лекарство от давления, может таким образом подавлять чувствительные штаммы бактерий своего микробиома и способствовать размножению и процветанию резистентных штаммов.
С другой стороны, результаты исследования позволяют предположить, что некоторые препараты, не являющиеся антибиотиками, можно будет перепрофилировать и применять в качестве таковых.
Например, ученые установили, что ряд препаратов подавляли рост такой болезнетворной бактерии, как Clostridium difficile, и это можно будет использовать при избыточном росте клостридии.
Кроме того, находки немецких ученых ставят перед фармацевтической наукой еще одну непростую задачу – усовершенствовать препараты, снизив их побочные эффекты.
А теперь – хорошие новости.
Малацидин – «убивающий плохое»

Так назвала новый антибиотик команда ученых университета Рокфеллера (Нью-Йорк, США), которым удалось выделить его из почвы. В названии было использовано удачное совпадение: mala означает по-латыни «плохой» и в то же время – это аббревиатура от metagenomic acidic lipopeptide antibiotic, то есть «метагеномный кислотообразующий липопептидный антибиотик», каковым малацидин и является.
Результаты исследования американских ученых были опубликованы в феврале 2018 года.
Эффективность малацидина проверили на подопытных животных. Его ввели лабораторным крысам, зараженным метициллинрезистентным золотистым стафилококком (MRSA), одним из самых устойчивых и распространенных патогенных штаммов, по праву считающимся супербагом.
Ученые наблюдали, как под действием препарата разрушались стенки бактерий Staphylococcus aureus, причем излечение произошло в первые же сутки введения препарата.
Что особенно важно, при повторных применениях бактерии не смогли выработать устойчивости к малацидину.
До клинических испытаний на человеческой модели пока что далеко, но препарат весьма многообещающий. Ученые работают над созданием синтетической версии малацидина и одновременно – над поиском его аналогов в природе, имея в виду ресурсы для его массового производства в будущем.
Но исследователи ищут новые антибактериальные агенты не только в почве. Следующим героем истории борьбы с супербагами становится экзотическое животное.
Подоить утконоса
Утконос (Ornithorhynchus anatinus) – австралийское млекопитающее, по ряду признаков близкое к рептилиям и птицам, что делает его уникальным. Самка утконоса кладет яйца, но выкармливает детеныша молоком. Утконос теплокровный, покрыт густым и мягким мехом, но обладает при этом клювом, позволяющим искать пищу в иле, за что и получил свое название.
Кто бы мог подумать, что это необычное животное может помочь человечеству в борьбе с супербагами? Эта идея принадлежит австралийским ученым.
Их логика вполне убедительна. Дело в том, что молочные железы самки утконоса лишены соска, и ее младенцы не сосут, а слизывают выделяющееся из желез молоко с материнской шерсти, кишащей разнообразными микроорганизмами. Чтобы защитить малышей, молоко должно обладать антибактериальными свойствами.
Впервые эти свойства были обнаружены группой ученых из нескольких научных институтов Австралии в 2011 году (вот их исследование).
Пептиды, выделенные из молока утконоса, оказались действенными против широкого спектра бактерий, как грамположительных, включая золотистый стафилококк Staphylococcus aureus, так и грамотрицательных (например, Escherichia coli, и Salmonella choleraesuis).
А совсем недавно ученые Научной и промышленной исследовательской организации Содружества наций вместе с университетом Дикина (Виктория) предприняли попытку воспроизвести белок молока утконоса, обладающий антибактериальными свойствами.
Это непростая задача, но с помощью современного оборудования и технологий специалистам удалось это сделать. Их исследование было опубликовано в январе 2018 года.
Возможно, антибактериальные свойства белка объясняются его необычной 3-D структурой. По форме он напоминает локон, поэтому ученые прозвали его «Шерли Темпл», по имени голливудской актрисы. (В 30-е годы ХХ века она снималась в детских ролях, будучи очень востребованной благодаря своей привлекательной внешности, важной частью которой были пышные локоны). Белок такой формы ученые встретили в природе впервые.
Ученые очень надеются, что «Шерли Темпл» в скором времени вступит в войну с антибиотикорезистентностью и победа окажется на ее стороне.
Однако на этом экзотика не заканчивается.
DRGN-1 – антибактериальный агент из крови комодского варана

Идея использовать его в качестве источника принадлежит американским ученым из университета Джорджа Мейсона (Манассас, США).
Ученые заметили, что эта рептилия, обитающая на островах Индонезии, почти не болеет, несмотря на то, что питается падалью, кишащей патогенами.
В чем же секрет крепкого здоровья комодского варана? Исследователи объясняют его содержащимся в его крови пептидом VK25, который им удалось выделить из образца крови животного-резидента Зоологического парка фермы аллигаторов имени Святого Августина во Флориде.
Оказалось, что данный пептид обладает мягким антимикробным действием и, что чрезвычайно важно, способен предотвратить формирование биопленки, которую образуют слипающиеся друг с другом микроорганизмы, после чего их колонию очень трудно разрушить. Именно биопленка является одной из причин, почему так трудно бороться с раневыми инфекциями.
Для повышения эффективности агента VK25 ученые произвели рекомбинацию входящих в него аминокислот. Полученный синтетический пептид исследователи назвали DRGN-1. Он обладает более сильным антибактериальным действием и более стабилен, чем собственный пептид варана.
Следующим шагом стало испытание препарата на раненых мышах, инфицированных двумя резистентными штаммами бактерий Pseudomonas aeruginosa и Staphylococcus aureus. Синтетический пептид сначала разрушил биопленку в ранах, а затем и убил патогены.
Ученые планируют на основе DRGN-1 создать мазь для заживления ран животных, а затем надеются применить синтетический пептид в разработке лекарственных средств для человека.
Будет ли побеждена антибиотикорезистентность? Окончательного ответа сегодня нет, но надежда есть. Во всяком случае, у науки очень хорошие шансы достичь поставленной цели.
Источники:
Study: Non-antibiotic drugs affect gut bacteria, could promote resistance
Platypus milk: The key to preventing deadly infections?
A new antibiotic Malacidin from soil kills resistant bacteria



