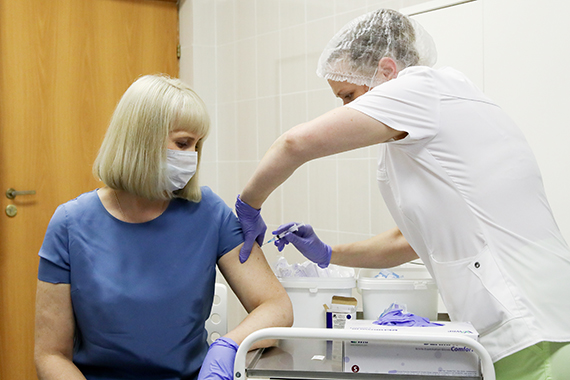
Вакцина для чрезвычайной ситуации
Распространение коронавируса в России вновь ускорилось, 21 сентября было зафиксировано 6196 случаев инфицирования.
Вакцина против коронавируса SARS-CoV-2, разработанная в НИЦ эпидемиологии и микробиологии имени Н.Ф.Гамалеи, проходит III фазу клинических исследований, которая продлится полгода. В исследованиях участвуют 40 тысяч добровольцев. Препарат «Спутник V» (или ГамКовидВак) был зарегистрирован 12 августа, после совмещенных I и II фазы клинических испытаний всего на 76 добровольцах. Обычно к участию во II фазе исследований привлекают сотни людей.
Ускоренную процедуру регистрации допустили в соответствии с постановлением правительства № 441, принятым в апреле этого года. Документ разрешает в чрезвычайных ситуациях (или для их предотвращения) регистрировать препараты на основе неполных данных клинических исследований.
Регистрационное удостоверение вакцины ГамКовидВак, как и само постановление правительства, действительно до 1 января 2021 года. Скорее всего, регистрация будет продлена, сказала в интервью «Милосердию.ru» Светлана Завидова, исполнительный директор Ассоциации организаций по клиническим исследованиям (АОКИ).
С 12 сентября началась поставка препарата в российские регионы для вакцинации групп риска, в первую очередь медиков и учителей. Массовая прививочная кампания может начаться в конце года, передает «Интерфакс» со ссылкой на слова министра здравоохранения РФ Михаила Мурашко.
«Делают прививку в условиях эпидемии и смотрят, кто заразился»
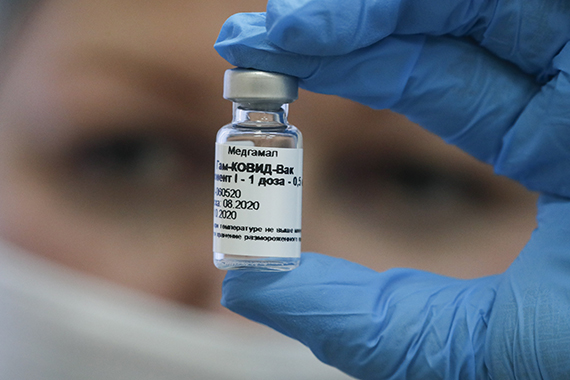
Итак, вакцина готова, утверждают разработчики. Можно ли идти прививаться?
«Защитные свойства вакцины проверяются, упрощенно говоря, так: людям делают прививку в условиях эпидемии и смотрят, заразился кто-то из них, или нет. В статье разработчиков ГамКовидВак, опубликованной в научном журнале The Lancet, такой вопрос пока даже не ставится. На него пока нет ответа.
Защитные свойства препарата еще предстоит изучить в третьей фазе испытаний», – отметил в интервью «Милосердию.ru» Сергей Нетесов, член-корреспондент РАН, заведующий лабораторией биотехнологии и вирусологии Новосибирского государственного университета.
Ученые НИЦ им. Гамалеи только 4 сентября поделились с научным сообществом результатами I и II фазы клинических исследований своей вакцины – в одном из самых известных медицинских изданий мира, журнале The Lancet. До этого они сообщали о своей работе лишь в формате интервью и пресс-конференций.
В статье, в частности, приводятся подробные данные о количестве антител к коронавирусу, образовавшихся у привитых добровольцев. Их число в 1,5 раза превышает уровень антител у людей, переболевших COVID-19, подчеркнул в своей колонке для агентства Sputnik Кирилл Дмитриев, генеральный директор Российского фонда прямых инвестиций (партнер НИЦ им. Гамалеи в разработке и производстве вакцины).
Но иммуногенность и эффективность вакцины – это далеко не одно и то же. Десятки вариантов вакцин против ВИЧ и гепатита C, которые пытались создать ученые в разных странах, тоже давали и антитела, и клеточный иммунный ответ, но защиты от инфекции не обеспечивали, отметил Сергей Нетесов.
«Что толку защищать молодых и здоровых?»
Безопасность вакцины «Спутник V» (она же ГамКовидВак) уже доказана, заявил в ходе онлайн-брифинга 10 сентября заместитель директора НИЦ им. Гамалеи по научной работе Денис Логунов (его цитирует ТАСС).
Согласно публикации в журнале The Lancet, в ходе I и II фазы клинических испытаний 44 добровольца (58%) ощущали боль в месте инъекции, у 38 (50%) поднялась температура, 32 (42%) жаловались на головную боль, 18 (24%) – на боль в мышцах и суставах.
По данным на 15 сентября, которые обнародовал министр здравоохранения РФ Михаил Мурашко, около 14% добровольцев, получивших прививку от коронавируса в рамках III фазы испытаний, жалуются на слабость, температуру и боли в мышцах.
«Надо всегда оговаривать, для кого безопасна вакцина, – отметил Сергей Нетесов. – Для участия в I и II фазе испытаний отобрали 76 здоровых молодых людей. Да, для них вакцина оказалась почти безопасна. Почти – потому что повышение температуры все-таки о чем-то говорит.
При самом заболевании температура далеко не всегда поднимается до 38 градусов. Два дня температура 37 градусов и потеря обоняния и вкуса на неделю – вот нередкие симптомы коронавирусной инфекции у здоровых молодых людей. Не менее чем в 40% случаев инфекция проходит вообще бессимптомно.
Уязвимая группа, которая действительно тяжело переносит COVID-19, – пожилые люди и люди с хроническими заболеваниями. Именно их в первую очередь и должна защищать вакцина. Что толку защищать здоровых людей?
Они и так легко перенесут это заболевание. Но безопасность вакцины для пожилых людей еще только начали изучать».
Людей старше 60 лет привлекут к участию в клинических исследованиях во время III фазы, сообщил «Известиям» директор НИЦ имени Гамалеи Александр Гинцбург.
Сергей Нетесов не рекомендовал бы пожилым людям спешить с вакцинацией. Лучше подождать результатов III фазы клинических испытаний, считает он.
Эффективность проверяли в Гвинее, но после эпидемии

Основной аргумент разработчиков в пользу ускоренной разработки вакцины – «проверенная» аденовирусная платформа с «доказанной» эффективностью. На ее основе уже создана вакцина от лихорадки Эбола, которая применялась в Гвинее, и вакцина от ближневосточного респираторного синдрома (MERS), прошедшая I и II фазы клинических испытаний. В сумме эти две вакцины с 2015 года получили более трех тысяч человек, сообщил Кирилл Дмитриев.
«Результаты III фазы клинических испытаний вакцины от лихорадки Эбола, проводившейся в Гвинее, не были опубликованы, – отметил Сергей Нетесов.
– Доклиническая разработка вакцины завершилась в конце 2015 года. А вспышка лихорадки Эбола в Гвинее, Сьерра-Леоне и Либерии закончилась летом 2015 года. То есть, проверить эффективность вакцины было невозможно.
Следующая вспышка заболевания началась в Демократической республике Конго. Там российская вакцина не применялась, туда успели попасть только две американские компании: Johnson & Johnson и Merck Sharp & Dohme (MSD).
Первая успела привить около 50 тысяч людей, а вторая – около 300 тысяч. По предварительным результатам, никто из людей, привитых вакциной MSD, не заболел лихорадкой Эбола. Результатов применения вакцины Johnson & Johnson я не видел».
По мнению Сергея Нетесова, достоинства российской разработки преподносятся общественности с неуместной пока «помпой».
Например, компания MSD, действительно доказавшая эффективность своей вакцины против лихорадки Эбола, тоже разрабатывает на ее платформе вакцину против коронавируса. «Но клинические исследования препарата проходят по всем правилам. Закончилась I фаза, начинается II. Часть добровольцев уже на II фазе набрали из людей пожилого возраста, но никакого бурления в СМИ по этому поводу нет», – сказал эксперт.
За добровольца – 2 миллиона, за обычного гражданина – 30 тысяч
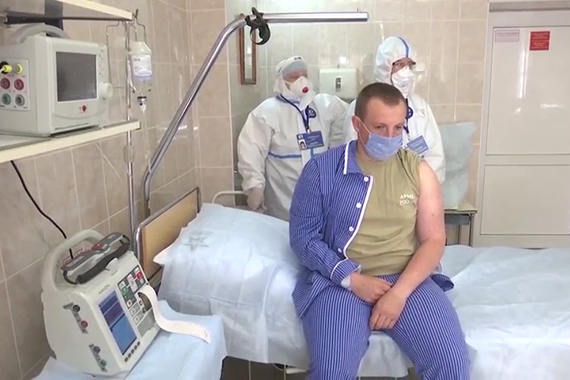
Почему участвовать в клинических исследованиях ГамКовидВак менее рискованно, чем сделать эту же прививку вместе с группами риска? «Состояние здоровья добровольцев, участвующих в испытаниях вакцины, проверяется очень тщательно, – сказал Сергей Нетесов. – За ними организовано наблюдение, они имеют право первоочередного обращения в больницу.
А человек, который сам вызвался сделать прививку, возьмет все риски на себя. Я считаю, что если вы хоть сколько-то себя любите и уважаете, то подождете результатов III фазы».
«В рутинной практике о компенсациях в случае осложнений от прививки, даже если они нанесли серьезный вред здоровью, речь не идет. Конечно, можно подать в суд на производителя вакцины, но доказать, что реакцию вызвал именно этот препарат, а не какое-то другое лекарство, очень сложно», – отметила Светлана Завидова.
Человек, сумевший доказать, что стал инвалидом из-за прививки, получает от государства 1000 рублей ежемесячно. В случае смерти гражданина его наследники могут отсудить у государства 30 тысяч рублей единовременно.
От производителя вакцины по решению суда можно получить порядка 800 тысяч рублей, рассказали «Милосердию.ru» юристы.
Но добровольцам судиться не придется. С каждым участником клинических исследований заключается договор обязательного медицинского страхования. Согласно ФЗ «Об обращении лекарственных средств», в случае смерти добровольца в ходе испытаний вакцины его наследники получат 2 млн рублей. Установление инвалидности I группы обойдется государству в 1,5 млн рублей, II группы – 1 млн рублей, III группы – 0,5 млн рублей.
«Температура тела может повышаться от самовнушения»

В первые три дня после вакцинации каждый участник III фазы клинических исследований обязан регулярно заполнять анкету в специально созданном мобильном приложении, отвечая на вопросы о своем самочувствии. Затем в течение полугода сообщать нужно будет лишь о нежелательных явлениях.
Для сопровождения добровольцев был создан телемедицинский центр, пишет ТАСС со ссылкой на сообщение главы Минздрава. С помощью приложения каждый участник может связываться с врачом – оператором центра, имеющим доступ к его электронной медицинской карте.
Сведения обо всех реакциях и явлениях, которые заметят добровольцы и наблюдающие за ними врачи, будут передаваться в специальную информационную систему.
Состояние здоровья граждан из групп риска, которые пройдут вакцинацию вне рамок клинических исследований, тоже будут контролировать с помощью приложения, сообщил ранее «Интерфакс».
Однако информационная система не может быть единой для клинических испытаний и для массовой вакцинации, подчеркнула Светлана Завидова. «Во время клинических исследований невозможно понять, на что дается реакция, потому что неизвестно, кто получил вакцину, а кто – плацебо.
Данные сначала просто аккумулируются. Код участника вскрывается до окончания исследований лишь в том случае, если произошло что-то действительно серьезное», – объяснила она.
«В Европе и США участников клинических испытаний делят, как минимум, на три группы, – рассказал Сергей Нетесов. – Первая получает исследуемую вакцину. Вторая – аналогичную вакцину, например, от гриппа. Третья группа получает плацебо, обычно это физиологический раствор. Никто из добровольцев не знает, чем он привит.
По идее, так должны проводиться все фазы клинических испытаний. Потому что только так можно получить объективные данные. Ведь у некоторых людей температура тела повышается от самовнушения, а не от вакцины».
НИЦ им. Гамалеи начал проводить плацебо-контролируемое исследование лишь во время III фазы: 30 тысяч добровольцев получат ГамКовидВак, а 10 тысяч – плацебо. Об этом Александр Гинцбург сообщил ТАСС в начале сентября.
Сколько побочных эффектов допустимо для вакцины
Светлана Завидова назвала «лукавыми» данные о том, что нежелательная реакция отмечается лишь у 14% добровольцев. Поскольку четверть участников получает плацебо, процент на самом деле чуть больше. (Или же для разработчиков не является секретом, кто получил плацебо, а кто – вакцину?)
Все побочные эффекты и осложнения, возникающие у добровольцев, называют «нежелательными явлениями» и тщательно фиксируются. «В ходе анализа данных компания-разработчик оценивает полученные сообщения о нежелательных явлениях, классифицирует их по степени серьезности.
Если существует вероятность связи с приемом препарата, явление переносится в разряд “нежелательная реакция”, которая, в случае регистрации препарата, попадет в том числе в инструкцию по применению», – сказала Светлана Завидова.
«Рекомендации о приостановке исследования, о его продолжении или о внесении в него изменений дает независимый комитет по мониторингу данных. Обычно он создается по инициативе самой компании-спонсора (организации, ответственной за проведение исследований)», – добавила она.
Например, компания AstraZeneca временно приостановила, а затем возобновила клинические исследования вакцины против коронавируса, после того как у одного из участников диагностировали острый поперечный миелит.
«Возможно, там вскрыли коды и выяснили, что заболевший доброволец принимал плацебо. Возможно, эксперты изучили его историю болезни и нашли факты, доказывающие, что заболевание не связано с вакциной», – сказала Светлана Завидова.
Универсальной шкалы для принятия таких решений не существует. «В 1956–1962 гг. прием беременными женщинами талидомида (успокаивающее средство) привел к рождению тысяч детей с тяжелыми физическими дефектами, – напомнила исполнительный директор АОКИ. – Однако действующее вещество этого препарата используется до сих пор для лечения проказы и отдельных видов онкологических заболеваний. Вопрос в условиях применения, в соотношении риска и пользы».
Каждый вариант прививки испытали лишь на 20 добровольцах

Главный редактор журнала The Lancet Ричард Хортон (Richard Horton), комментируя публикацию статьи о российской вакцине, отметил, что результаты клинических исследований «Спутника V» «обнадеживают», однако говорить о готовности препарата к массовому применению «преждевременно». Причина – до сих пор в испытаниях приняли участие лишь 76 человек.
«По сути, в рутинную практику выпускают препарат, который прошел лишь I фазу клинических исследований, – отметила по этому поводу Светлана Завидова. – Несмотря на то, что официально прошедшие летом испытания относят к I и II фазам одновременно, каждый из вариантов прививки получили только 20 человек».
«Есть две формы вакцины, – пояснила она. – Раствор для внутримышечного введения и лиофилизат, то есть порошок для приготовления раствора. Поэтому проводилось два исследования, в каждом из которых участвовали по 38 человек. Раствор тестировали в госпитале имени Бурденко, а лиофилизат – в Сеченовском университете.
Кроме того, есть два компонента вакцины, которые вводятся с разницей в 21 день (в первом вектором является аденовирус 26-го серотипа, во втором – 5-го серотипа). В каждом из исследований на первом этапе 9 человек получили первый компонент, а другие 9 человек – второй.
Разработчики посмотрели, как добровольцы реагируют. Затем 20 человек получили уже оба компонента с разницей в 21 день. Получается, в полном объеме каждую форму вакцины получили только 20 человек».
До сих пор различий между российскими и международными стандартами проведения клинических исследований не существовало, отметила Светлана Завидова. Отклонение от правил при испытаниях вакцины ГамКовидВак произошло в соответствии с постановлением правительства № 441, которое упрощает регистрацию препаратов в чрезвычайных обстоятельствах.
11 сентября «Милосердие.ru» обратилось в НИЦ им. Гамалеи с просьбой разъяснить, что безопаснее для пожилых людей и лиц с хроническими заболеваниями: привиться при первой возможности, или подождать окончания III фазы клинических исследований. На момент публикации текста ответа мы не получили.